新型コロナウイルスへのファビピラビル、ナファモスタット、クロロキンなど最新治療薬情報
We manage version control so you can make changes on the fly. Sophisticated options allow you to set the QA score rules and policies. Engage agents via dashboards A well designed quality process will only work if your agents engage with and trust the tools. Collaboration, transparency and communication are at the heart of Scorebuddy enabling real, measurable change to take place delivering consistently improving customer experiences. Scorebuddy allows you to highlight and share patterns and trends across groups and teams, drilling all the way down as far as the individual agent. And what if you could brand the survey for your company and link the result to the agent? Easy to deploy• Quick to deploy• Immediate results delivered to the agent and the team The first step we took as part of our QA strategy, was to decide what platform would be used that would provide analytics and reporting that we could do with ease. We needed to make sure we could access the data easily. We selected Scorebuddy! For Outsourcers working with a scorecard system like Scorebuddy, the primary problem is that you take the ecosystem that your clients use when they come on board. Scorebuddy can be used to standardize to one way of capturing quality, regardless of the ecosystem being used by the client. The 1 Outsourcer challenge is too much work and too little time. If used properly, Scorebuddy gives you the gift of time! At Beachbody we manage call centers on a global level and we use Scorebuddy to manage all of our QA Teams. Our QA teams randomly sample agent interactions, auditing all channels including voice, chat, email and social. We find Scorebuddy extremely easy to use, the look and feel is very user friendly. Our agents can review their dashboards immediately, reviewing feedback and gauging where they stand against other agents in real-time. Another major benefit of using Scorebuddy is due to their extensive and unique compliance suite. Furthermore, the team at Scorebuddy has been incredible, as far as when we need to reach out, requesting any type of assistance with a problem. Everyone has always been very attentive, so that has been incredible. Ryanair initially used Scorebuddy to measure 600 staff and 3 outsource partners throughout Europe. The value was seen immediately as our quality team saved hours every week by not having to struggle with the process via spreadsheets, and the team has found it easy to use. This requires a lot of emphasis on creating unique scorecards to cater to those different cultures and languages. Furthermore, we are currently getting ready to go live with our Zendesk integration. Scorebuddy has provided BenefitMall with an application for building consistent and customer focused quality evaluation solutions across business units and locations. Our front line now depends on Scorebuddy as an integral part of performance development tools used with staff. This includes over 400 users along with 80 admins and supervisors, which is why utilizing Agent Insights is essential for our business. By using Agent Dashboards agents feel more involved and the team is more aligned on what quality level is expected, especially the self-scoring and the option to request a 1:1 are really paying off. Using the Analytics reports provide us with information where to focus on, the loop with training and coaching is easily made and we can improve our tools to support our agents in a better way. The Scorebuddy-Zendesk Integration saves us a lot of manual work and that definitely is a plus, which in turn makes the overall QA process more efficient. Staff lists are up to date, unlike their previous system which was only updated annually. The managers have increased autonomy and ownership over their quality forms as they can instantly change their scorecards to what suits their needs. Some of our favourite features of the Scorebuddy enterprise package are Agent Insights and Analytics, which allow us to gain foresight into trends that impact our day to day business.
次の
Call Center Quality Measurement & Agent Engagement Solution

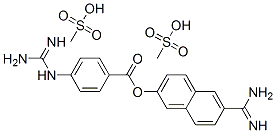
UpToDate Contents 全文を閲覧するには購読必要です。 To read the full text you will need to subscribe. hemodialysis anticoagulation• anticoagulation for continuous renal replacement therapy• post endoscopic retrograde cholangiopancreatography ercp pancreatitis• serum enzymes in patients with renal failure Related Links• 注射用ナファタット。 持田製薬株式会社の提供する医療関係者のためのホームページです。 医薬品の写真、服用の手引き、注意事項などの製品情報がご覧になれます。 PDFファイルの閲覧には、 Adobe Reader が必要です。 Related Pictures Japan Pharmaceutical Reference 薬効分類名• 蛋白分解酵素阻害剤 販売名 注射用ナファタット100 組成 注射用ナファタット100• 1バイアル中ナファモスタットメシル酸塩100mgを含有する。 添加物としてD-マンニトール200mg,pH調節剤を含有する。 本剤の成分に対し過敏症の既往歴のある患者 効能または効果• 汎発性血管内血液凝固症(DIC)• 出血性病変又は出血傾向を有する患者の血液体外循環時の灌流血液の凝固防止(血液透析及びプラスマフェレーシス) 汎発性血管内血液凝固症(DIC)に使用する場合• 通常,1日量を5%ブドウ糖注射液1,000mLに溶解し,ナファモスタットメシル酸塩として毎時0. 06〜0. 20mg/kgを24時間かけて静脈内に持続注入する。 出血性病変又は出血傾向を有する患者の血液体外循環時の灌流血液の凝固防止に使用する場合• 通常,体外循環開始に先だち,ナファモスタットメシル酸塩として20mgを生理食塩液500mLに溶解した液で血液回路内の洗浄・充てんを行い,体外循環開始後は,ナファモスタットメシル酸塩として毎時20〜50mgを5%ブドウ糖注射液に溶解し,抗凝固剤注入ラインより持続注入する。 なお,症状に応じ適宜増減する。 注射液の調製法• 本剤の使用にあたっては以下の手順で注射液を調製すること。 汎発性血管内血液凝固症(DIC)に使用する場合• 本剤1バイアルに10mL以上の5%ブドウ糖注射液又は注射用水を加え,完全に溶解する。 溶解した液を5%ブドウ糖注射液に混和する。 出血性病変又は出血傾向を有する患者の血液体外循環時の灌流血液の凝固防止に使用する場合 血液回路内の洗浄・充てん• 本剤1バイアルに10mLの5%ブドウ糖注射液又は注射用水を加え,完全に溶解する。 ナファモスタットメシル酸塩20mgを含む溶解液を生理食塩液に混和する。 体外循環時• 本剤1バイアルに10mLの5%ブドウ糖注射液又は注射用水を加え,完全に溶解する。 溶解した液を抗凝固剤持続注入器の容量に合わせ,5%ブドウ糖注射液で希釈する。 溶解時の注意• 白濁あるいは結晶が析出する場合があるので,生理食塩液又は無機塩類を含有する溶液をバイアルに直接加えないこと。 重大な副作用 ショック,アナフィラキシー様症状(頻度不明)• ショック,アナフィラキシー様症状があらわれることがあるので,観察を十分に行い,血圧低下,意識障害,呼吸困難,気管支喘息様発作,喘鳴,胸部不快,腹痛,嘔吐,発熱,冷汗,そう痒感,紅潮,発赤,しびれ等があらわれた場合には直ちに投与を中止し,適切な処置を行うこと。 高カリウム血症(頻度不明)• 高カリウム血症があらわれることがあるので,カリウム含有製剤(輸液等),カリウム保持性利尿剤等を併用する場合には,特に観察を十分に行い,異常が認められた場合には直ちに投与を中止し,適切な処置を行うこと。 なお,高カリウム血症の発現によって不整脈を誘発した例が報告されている。 低ナトリウム血症(頻度不明)• 低ナトリウム血症があらわれることがあるので,異常が認められた場合には直ちに投与を中止し,適切な処置を行うこと。 血小板減少(頻度不明)• 血小板減少があらわれることがあるので,血液検査等の観察を十分に行い,異常が認められた場合には投与を中止し,適切な処置を行うこと。 白血球減少(頻度不明)• 白血球減少があらわれることがあるので,血液検査等の観察を十分に行い,異常が認められた場合には投与を中止し,適切な処置を行うこと。 肝機能障害,黄疸(頻度不明)• 有効成分に関する理化学的知見 一般名• ナファモスタットメシル酸塩(Nafamostat Mesilate) 化学名• 6-Amidinonaphthalen-2-yl 4-guanidinobenzoate bis(methanesulfonate) 分子式• C 19H 17N 5O 2・2CH 4O 3S 分子量• 539. 58 性状• 白色の結晶性の粉末である。 ギ酸に溶けやすく,水にやや溶けやすく,エタノール(99. 5)にほとんど溶けない。 本品は0. 01mol/L塩酸試液に溶ける。 「 英 化 商 、、、、、、、、、、、、、、 分類• 蛋白分解酵素阻害薬• 膵炎治療薬• 膵プロテアーゼ阻害薬 構造 作用機序• トロンビン、活性型凝固因子、カリクレイン、プラスミン、補体、トリプシンなどの蛋白分解酵素を強力に阻害するとともに血小板凝集を抑制 薬理作用 薬効薬理 注射用フサン50• 酵素阻害作用18 ~25• 本品はトロンビン、活性型凝固因子(XIIa、Xa、VIIa)、カリクレイン、プラスミン、補体(C1r-、C1s-)、トリプシン等の蛋白分解酵素を強力に阻害し、ホスホリパーゼA2に対しても阻害作用を示す。 トロンビンに対する阻害作用は、ATIIIを介さずに発現する。 実験的急性膵炎に対する作用23 ,26• 本品はトリプシン、エンテロキナーゼ及びエンドトキシンを膵管内に逆行性に注入して惹起した各種実験的膵炎に対し、死亡率を低下させる(ラット、ウサギ)。 血液凝固時間延長作用22 ,27 ,28• 本品は各種凝固時間(APTT、PT、TT、LWCT、CCT)を延長させる(in vitro)。 血小板凝集抑制作用27)• 本品はトロンビン、アドレナリン、ADP、コラゲン及びエンドトキシンによる血小板凝集を抑制する(in vitro)。 実験的DICに対する作用29 ~31)• 本品はエンドトキシン投与による実験的DICに対し、各種凝血学的検査値を改善し、腎糸球体のフィブリン血栓形成を抑制する(ラット、ウサギ)。 体外循環路内の抗凝固作用2 ,17 ,28• 本剤を血液透析及びプラスマフェレーシスの抗凝固薬として使用したとき、血中濃度に相関した血液凝固時間の延長が体外循環路内にほぼ限局して認められた(ヒト)。 カリクレイン-キニン系に対する作用19 ,32• 本品は静脈内投与後採取した血漿において、ガラス粉によるキニン生成を抑制する(ラット)。 本剤を膵炎患者に投与した結果、カリクレインの活性化に基づく総キニノゲン量の減少が改善された。 補体系に対する作用19• 本品は補体溶血反応を抑制する(in vitro)。 動態 適応• 膵炎の急性症状の改善、播種性血管内血液凝固症候群 DIC 、出血性病変・出血傾向を有する患者の血液体外循環時の灌流血液の凝固防止 効能又は効果 注射用フサン50• 汎発性血管内血液凝固症(DIC)• 出血性病変又は出血傾向を有する患者の血液体外循環時の灌流血液の凝固防止(血液透析及びプラスマフェレーシス) 禁忌• 過敏症既往 副作用• ショック、高カリウム血症・低ナトリウム血症 相互作用 添付文書• コアヒビター注射用10mg/コアヒビター注射用50mg/コアヒビター注射用100mg/コアヒビター注射用150mg [display]• 注射用フサン50 [display].
次の
S&V⇒料理

UpToDate Contents 全文を閲覧するには購読必要です。 To read the full text you will need to subscribe. hemodialysis anticoagulation• post ercp pancreatitis• serum enzymes in patients with renal failure Related Links• Related Pictures Japan Pharmaceutical Reference 薬効分類名• 日本薬局方 ナファモスタットメシル酸塩 10mg 添加物(1バイアル中)• D-マンニトール 適量 添加物(1バイアル中)• コハク酸 適量 禁忌• 本剤の成分に対し過敏症の既往歴のある患者 効能または効果 注射用ナモスタット10mg• 膵炎の急性症状(急性膵炎、慢性膵炎の急性増悪、術後の急性膵炎、膵管造影後の急性膵炎、外傷性膵炎)の改善 注射用ナモスタット10mg・50mg(共通)• 汎発性血管内血液凝固症(DIC) 注射用ナモスタット10mg・50mg(共通)• 出血性病変又は出血傾向を有する患者の血液体外循環時の灌流血液の凝固防止(血液透析及びプラスマフェレーシス) 注射用ナモスタット10mg (効能・効果)膵炎の急性症状(急性膵炎、慢性膵炎の急性増悪、術後の急性膵炎、膵管造影後の急性膵炎、外傷性膵炎)の改善• (用法・用量)通常、1回、ナファモスタットメシル酸塩として10mgを5%ブドウ糖注射液500mLに溶解し、約2時間前後かけて1日1〜2回静脈内に点滴注入する。 なお、症状に応じ適宜増減する。 注射用ナモスタット10mg・50mg(共通) (効能・効果)汎発性血管内血液凝固症(DIC)• (用法・用量)通常、1日量を5%ブドウ糖注射液1,000mLに溶解し、ナファモスタットメシル酸塩として毎時0. 06〜0. 注射用ナモスタット10mg・50mg(共通) (効能・効果)出血性病変又は出血傾向を有する患者の血液体外循環時の灌流血液の凝固防止(血液透析及びプラスマフェレーシス)• (用法・用量)通常、体外循環開始に先だち、ナファモスタットメシル酸塩として20mgを生理食塩液500mLに溶解した液で血液回路内の洗浄・充てんを行い、体外循環開始後は、ナファモスタットメシル酸塩として毎時20〜50mgを5%ブドウ糖注射液に溶解し、抗凝固剤注入ラインより持続注入する。 なお、症状に応じ適宜増減する。 注射液の調製法• 本剤の使用にあたっては以下の手順で注射液を調製すること。 膵炎の急性症状の改善に使用する場合• 10mgバイアルに1mL以上の5%ブドウ糖注射液又は注射用水を加え、完全に溶解する。 溶解した液を5%ブドウ糖注射液に混和する。 汎発性血管内血液凝固症(DIC)に使用する場合• 10mgバイアルには1mL以上、50mgバイアルには5mL以上の5%ブドウ糖注射液又は注射用水を加え、完全に溶解する。 溶解した液を5%ブドウ糖注射液に混和する。 出血性病変又は出血傾向を有する患者の血液体外循環時の灌流血液の凝固防止に使用する場合 血液回路内の洗浄・充てん• 10mgバイアルには1mL、50mgバイアルには5mLの5%ブドウ糖注射液又は注射用水を加え、完全に溶解する。 ナファモスタットメシル酸塩20mgを含む溶解液を生理食塩液に混和する。 体外循環時• 10mgバイアルには1mL、50mgバイアルには5mLの5%ブドウ糖注射液又は注射用水を加え、完全に溶解する。 溶解した液を抗凝固剤持続注入器の容量に合わせ、5%ブドウ糖注射液で希釈する。 溶解時の注意• 白濁あるいは結晶が析出する場合があるので、生理食塩液又は無機塩類を含有する溶液をバイアルに直接加えないこと。 重大な副作用 ショック、アナフィラキシー様症状 頻度不明• ショック、アナフィラキシー様症状があらわれることがあるので、観察を十分に行い、血圧低下、意識障害、呼吸困難、気管支喘息様発作、喘鳴、胸部不快、腹痛、嘔吐、発熱、冷汗、そう痒感、紅潮、発赤、しびれ等があらわれた場合には直ちに投与を中止し、適切な処置を行うこと。 高カリウム血症 頻度不明• 高カリウム血症があらわれることがあるので、カリウム含有製剤 (輸液等)、カリウム保持性利尿剤等を併用する場合には、特に観察を十分に行い、異常が認められた場合には直ちに投与を中止し、適切な処置を行うこと。 なお、高カリウム血症の発現によって不整脈を誘発した例が報告されている。 低ナトリウム血症 頻度不明• 低ナトリウム血症があらわれることがあるので、異常が認められた場合には直ちに投与を中止し、適切な処置を行うこと。 血小板減少 頻度不明• 血小板減少があらわれることがあるので、血液検査等の観察を十分に行い、異常が認められた場合には投与を中止し、適切な処置を行うこと。 白血球減少 頻度不明• 白血球減少があらわれることがあるので、血液検査等の観察を十分に行い、異常が認められた場合には投与を中止し、適切な処置を行うこと。 肝機能障害、黄疸 頻度不明• 有効成分に関する理化学的知見• 「 英 化 商 、、、、、、、、、、、、、、 分類• 蛋白分解酵素阻害薬• 膵炎治療薬• 膵プロテアーゼ阻害薬 構造 作用機序• トロンビン、活性型凝固因子、カリクレイン、プラスミン、補体、トリプシンなどの蛋白分解酵素を強力に阻害するとともに血小板凝集を抑制 薬理作用 薬効薬理 注射用フサン50• 酵素阻害作用18 ~25• 本品はトロンビン、活性型凝固因子(XIIa、Xa、VIIa)、カリクレイン、プラスミン、補体(C1r-、C1s-)、トリプシン等の蛋白分解酵素を強力に阻害し、ホスホリパーゼA2に対しても阻害作用を示す。 トロンビンに対する阻害作用は、ATIIIを介さずに発現する。 実験的急性膵炎に対する作用23 ,26• 本品はトリプシン、エンテロキナーゼ及びエンドトキシンを膵管内に逆行性に注入して惹起した各種実験的膵炎に対し、死亡率を低下させる(ラット、ウサギ)。 血液凝固時間延長作用22 ,27 ,28• 本品は各種凝固時間(APTT、PT、TT、LWCT、CCT)を延長させる(in vitro)。 血小板凝集抑制作用27)• 本品はトロンビン、アドレナリン、ADP、コラゲン及びエンドトキシンによる血小板凝集を抑制する(in vitro)。 実験的DICに対する作用29 ~31)• 本品はエンドトキシン投与による実験的DICに対し、各種凝血学的検査値を改善し、腎糸球体のフィブリン血栓形成を抑制する(ラット、ウサギ)。 体外循環路内の抗凝固作用2 ,17 ,28• 本剤を血液透析及びプラスマフェレーシスの抗凝固薬として使用したとき、血中濃度に相関した血液凝固時間の延長が体外循環路内にほぼ限局して認められた(ヒト)。 カリクレイン-キニン系に対する作用19 ,32• 本品は静脈内投与後採取した血漿において、ガラス粉によるキニン生成を抑制する(ラット)。 本剤を膵炎患者に投与した結果、カリクレインの活性化に基づく総キニノゲン量の減少が改善された。 補体系に対する作用19• 本品は補体溶血反応を抑制する(in vitro)。 動態 適応• 膵炎の急性症状の改善、播種性血管内血液凝固症候群 DIC 、出血性病変・出血傾向を有する患者の血液体外循環時の灌流血液の凝固防止 効能又は効果 注射用フサン50• 汎発性血管内血液凝固症(DIC)• 出血性病変又は出血傾向を有する患者の血液体外循環時の灌流血液の凝固防止(血液透析及びプラスマフェレーシス) 禁忌• 過敏症既往 副作用• ショック、高カリウム血症・低ナトリウム血症 相互作用 添付文書• コアヒビター注射用10mg/コアヒビター注射用50mg/コアヒビター注射用100mg/コアヒビター注射用150mg [display]• 注射用フサン50 [display].
次の


